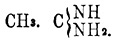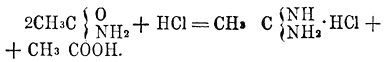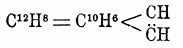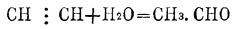(Acer L., клен) — род древовидных и кустарниковых растений,образующих с
несколькими экзотическими родами семейство Асеrinеае; характеризуется
супротивными, обыкновенно дланевидными листьями, в большинстве случаев
зеленовато-желтыми цветками, собранными в кисть или ложный зонтик, и двойными
крылатками, распадающимися при созревании на два односемянных плода. В
Европейской России, за исключением Крыма, растут 4 вида: A. tataricum L., A.
Pseudo-Platanus L., A. campestre L. и A. platanoides L., из которых только
последний вид пользуется обширным распространением (на С — до 62°). В Крыму
известны только: A. campestre L., A. Ualum Lauth. (A. opulifolium
Vill.) и A. platanoidecs L., Кавказ
же, напротив, чрезвычайно богат видами: здесь встречаются, кроме перечисленных,
A. Trautvetteri Medwed., A. insigne Boiss. et Buhse, A. hyrcanum Fisch, et Mey,
A. monspessulanum L., A. divergens C. Koch et Pax, A. Lobel i i
Ten (laetum C. A. Mey). — Близкий к A. Pseudo-Platanus вид, A. amliquum Heer,
известен из олигоцена в Гренландии и Шпицбергене и из миоцена на Сахалине, а в
плиоценовых отложениях он найден на Алтае. Здесь же найдены близкий к А. Lobelii
или тождественный с ним А. laetum С. А. Mey и A. Nordenskioldi Nath., который
Шмальгаузен соединяет с современным японским A. palmatum Thunb. — А tataricum
L., черноклен, кустарник с яйцевидными, иногда слегка трехлопастными
листьями и красными, вверх стоящими, почти параллельными между собой крыльями
плода; в черноземной полосе — до Волги (быть может, до Урала). — A. Pseudo-Platanus
L., явоp, дерево с пятилопастными, при основании сердцевидными листьями (лопасти
их коротко заостренные, неравномерно городчато-пильчатые) и зелеными цветками в
длинных висячих кистях; в западной и юго-западной России (см. таблицу Лиственные
деревья, фиг. 1, фиг. 2 и 3 — обоеполые цветки; 3 — по удалении чашечки и
венчика; 4 — мужской цветок; 5 — попечечный разрез завязи; 6 — крылатка; 7 —
часть ее в натуральную величину, налево вскрытая, чтобы показать семя; 8 —
вынутый зародыш; 9 — поперечный разрез семени по направлению а в фиг. 8; 10 —
верхушка побега зимой, с почками; 11 — выросшее из семени растение, с развитыми
семядолями как и первыми листьями). A. platanoides L., клен обыкновенный, дерево
с пятилопастными, при основании сердцевидными листьями (лопасти с почти
параллельными краями, длинно и тонко заостренные, с каждой стороны с 1 — 2
длиннозаостренными зубцами) и прямостоящими ложными зонтиками цветков — А.
campestre L., неклен,
наклен, кустарник или деревце с мелкими пятилопастными листьями (лопасти
цельные, тупые, иногда с несколькими крупными, тупыми зубцами) и прямостоящим
соцветием; растет в западной и юго-зап. России и на В приблизительно до Хопра. В
парках разводят иногда североамериканские виды — A. striatum L. (с полосатой
корой), A. negundo L. (с пестрыми листьями), A. dasycarpum Ehrh. (высокоствольное
дерево), A. rubrum L. и А. saccharinum Wangh. (nigrum Mich.), близкий к А. pla t anoides
и идущий в Америке на приготовление сахара. См. монографию о клене: Пакс (Ferd.
Pax), "Monographie der Gattung Acer" (в Englers "Botan. Jahrb ü chern",
т. VI, 1885, стр. 287 — 373 и т. VII, 1886, стр. 177 — 263). О распространении
кленов ср. Кёппен (Fr. Th. Koppen), "Geographische Verbreitung der
Holzgewachse des europä ischen
Russlands imd des Kaukasus" (1888 г.). |